A fajta kristályrétegeiben
A legtöbb szilárd anyag egy olyan kristályos szerkezettel, amelyet az jellemez, szigorúan meghatározott elrendezése a részecskék. Ha a részecskék kondicionált csatlakozni vonalak, megkapjuk a térbeli keret, az úgynevezett kristályrács. A pontok, ahol a részecske kristályrács nevű csomópontot. A csomópontok lehetnek képzeletbeli rács atomok. ionok vagy molekulák.
Jellegétől függően a részecskék, található a csomópontok, és a természet a kapcsolat négyféle kristályrétegeiben különböztetni őket ionos. fém. atomi és molekuláris.
Úgynevezett ionrácsos, amelyben ionok csomópontok.
Ezek az anyagok ionos kötést. Egy ilyen rácsos csomópontok elrendezett pozitív és negatív ionokat, amelyek egymással össze vannak kötve elektrosztatikus kölcsönhatás.
Az ionos sók kristályrácsban. lúg. aktív fém-oxidokat. Ionok lehetnek egyszerű vagy összetett. Például, egy nátrium-klorid kristályrács csomópontok egyszerű nátrium-ionok Na + és klór Cl -. és rácsos csomópontok kálium-szulfátot alternatív egyszerű káliumionok K + összetett és szulfátionok S O 4 2 -.
Kapcsolat között ionok ilyen szilárd kristályok formájában. Ezért, a szilárd ionos anyagok. tűzálló. nem illékony. Az ilyen anyagokat könnyen oldódik vízben.
A kristályrács nátrium-klorid

Crystal Nátrium-klorid
Fém úgynevezett rács, amely áll a pozitív ionok és a fématomok és a szabad elektronokat.
Alkotnak egy anyag egy fémes kötés. A fémes rács helyek atomok és ionok (atomok, hogy az ionok a könnyen átalakítható atomok, így a külső elektronok közös használatra).
Az ilyen kristályrács jellemző egyszerű anyagok fémek és ötvözetek.
fém olvadási hőmérsékletek különböző lehet (a \ (- 37 ° C \) a higany 2003 fok). De minden fémek jellegzetes fémes csillogás. alakíthatóság. alakíthatóság. magatartási elektromos áram és hő.
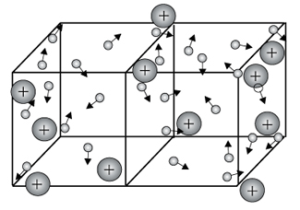
Metal kristályrács

Úgynevezett atomi kristályrács, a csomópontok, amelyek az egyes atomok kapcsolódik kovalens kötéssel.
Egy ilyen gyémánt rács típusú - a szénatomok egyike allotropic módosításokat. Anyagok atomi kristályrács jelentése szénatom. szilícium. bór és germánium. és komplex vegyületek, mint például a szilícium-karbid SiC és szilícium-dioxid. kvarc. strassz. homok. amelyek magukban foglalják a szilícium-oxid (IV) Si O 2.
Ezek az anyagok az jellemzi nagy szilárdság és a keménység. Így gyémánt a legkeményebb természetes anyag. Y anyagok atomi kristályrács nagyon magas olvadás- és forráspontja hőmérsékleten. Például, az olvadási hőmérsékletet szilika \ (1728 ° C \), míg magasabb grafit \ (4000 ° C \). Nukleáris gyakorlatilag oldhatatlan kristályokat.
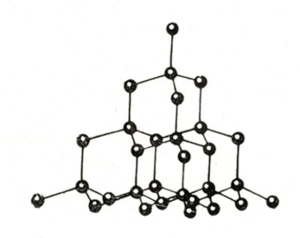
gyémánt kristályrács

Molekuláris rács nevezett, amelyben a csomópontok molekulák kapcsolódó gyenge intermolekuláris kölcsönhatást.
Annak ellenére, hogy a molekulák a atomok kapcsolódnak nagyon erős közötti kovalens kötések a molekulák maguk a gyenge intermolekuláris erők a vonzás. Ezért, a molekuláris kristályok alacsony szilárdság és a szívósság. alacsony olvadás- és forráspontja. Sok molekuláris anyag szobahőmérsékleten folyadékok és gázok. Az ilyen anyagok illékony. Például, kristályos szilárd jódot és a szén-oxid (IV) ( «szárazjég") elpárolognak nélkül megy át a folyékony állapotban. Néhány anyagnak molekuláris szaga.
Ez a típusú rostélyok egyszerű anyagok a szilárd halmazállapot: nemesgázok egyértékű molekulákkal (Ő Ne Ar Kr Xe Rn .....), Valamint a nemfémek di- vagy többértékű molekulák (H O 2. 2. 2. N Cl I O 2. 2. 3. 4. S P 8).
Molekuláris kristályrács is anyagok poláris kovalens kötés: a víz - jég. szilárd ammónia. sav. oxidok nem-fémek. A legtöbb szerves vegyületek is, amelyek molekuláris kristályok (naftalin. Cukor. Glükóz).
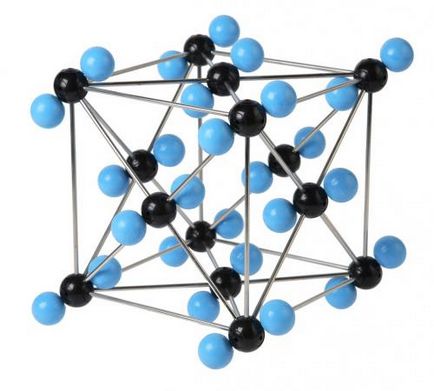
A kristályrács széndioxid